Faire croître des organes et des années de vie

Et si nos organes pouvaient un jour se reconstruire à mesure que l'usure ou la maladie les affectent?
Par Serge Beaucher
Prélevez quelques cellules humaines sur un petit échantillon d’épiderme, de gras ou de cordon ombilical. Cultivez-les avec une méthode adéquate et vous obtiendrez de grands morceaux de peau, des vaisseaux sanguins, des neurones ou même un morceau de cœur… De quoi régénérer certains tissus ou organes malades de la personne chez qui vous aurez extrait ces cellules.
Science-fiction? Non, science tout court! Comme celle qui se pratique dans les locaux de deux organismes de recherche de l’Université Laval: le Laboratoire d’organogénèse expérimentale (LOEX)1, né en 1985 et composé d’une cinquantaine de chercheurs et d’étudiants-chercheurs qui occupent tout un immeuble sur les terrains de l’hôpital de l’Enfant-Jésus, en plus de locaux de l’hôpital Saint-Sacrement à Québec; et le Laboratoire de biomatériaux et de bioingénierie (LBB)2du Département de génie des mines, de la métallurgie et des matériaux où, depuis 2000, s’activent une trentaine de chercheurs et d’étudiants-chercheurs.
Les travaux en génie tissulaire qu’on réalise dans ces laboratoires n’apporteront pas l’immortalité à l’être humain. Mais sans doute contribueront-ils à un allongement de l’espérance de vie.
Très certainement, en tout cas, à une amélioration de la qualité de vie de nombreuses personnes, assurent ceux qui y œuvrent.
C’est un travail de longue haleine, prévient toutefois Diego Mantovani3, le directeur du LBB: «Je comprends que les gens voudraient des solutions immédiates à leurs problèmes de santé, mais dans la plupart des cas, nous travaillons pour le futur, peut-être même pour les générations futures.»
1 Visitez le site du laboratoire. ↩
2 Visitez le site du laboratoire. ↩
3 Diego Mantovani est également membre du Centre québécois sur les matériaux fonctionnels et fondateur du Laboratoire international pour le développement des applications des matériaux en santé (LIDAMS). ↩
Un échafaudage biodégradable
Une partie des recherches du LBB porte sur des biomatériaux synthétiques, par exemple des prothèses artérielles (stents), ces petits ressorts métalliques qu’on insère dans les artères pour en éviter l’occlusion. Mais le Laboratoire est aussi très actif en génie tissulaire pour la reconstruction et la régénération de tissus vivants à partir des cellules souches d’un patient. Une cellule souche est une cellule indifférenciée qui peut se développer en divers types de cellules spécialisées: globules, neurones, cellules du foie, etc.
Pour produire un tissu vivant, il faut faire proliférer ces cellules. «Et leur fournir une structure sur laquelle échafauder leur prolifération, raconte Diego Mantovani. Une structure qui disparaîtra une fois les cellules transformées en tissu, comme les échafaudages utilisés pour construire une cathédrale sont enlevés quand le travail est terminé.»
Pour concevoir ces structures, différents laboratoires ont essayé toutes sortes de matériaux, depuis le fil d’araignée jusqu’aux polymères synthétiques à base de pétrole. L’échafaudage utilisé au LBB est un gel de collagène et d’élastine, des protéines animales que les chercheurs extraient de ligaments de queues de rats ayant d’abord servi à d’autres expériences. Quant aux cellules souches humaines qu’on intègre dans ce collagène pour leur permettre de s’y développer, elles sont prélevées sur des cordons ombilicaux donnés par des parents.
L’avantage du collagène
L’avantage du collagène par rapport à un échafaudage de protéines non animales: il est plus facile d’y faire adhérer et s’établir les cellules. La structure de collagène, sorte de filet gélatineux très mince constitué à plus de 95% d’eau, se dégrade rapidement dans le mélange; mais les cellules, «qui sont programmées pour construire leur maison», prennent le relais en commençant à produire leur propre collagène. Elles font donc le reste du travail elles-mêmes, explique M. Mantovani: «Nous leur fournissons les 2×4 et elles complètent l’œuvre. Si ce sont des cellules vasculaires, elles vont produire des tissus vasculaires, si ce sont des cellules cardiaques, elles produiront un morceau de cœur.»
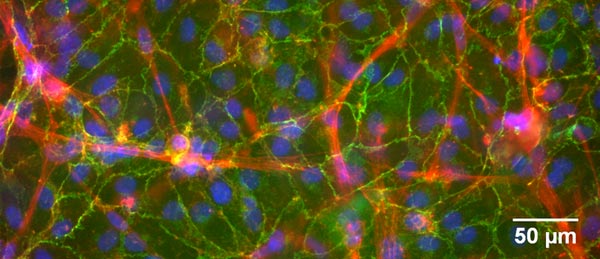
Photo Caroline Loy, Lucie Levesque et Diego Mantovani, www.lbb.ulaval.ca, 2014
Structure de collagène abritant une co-culture de cellules musculaires lisses (rouge) et de cellules endothéliales (vert)
Il faudra toutefois encore beaucoup de recherche avant que ce tissu soit aussi organisé que dans le corps humain, avec toutes les protéines et les interactions cellulaires nécessaires, de façon à pouvoir remplacer des artères ou réparer un organe malade. Pour l’instant, les grands défis sont de cultiver plusieurs types de cellules ensemble, de garder ces structures en vie longtemps et de produire tout cela à une échelle relativement grande. D’ici cinq ans, on aura fait un bout de chemin en ce sens, selon Diego Mantovani. «Mais nous serons encore loin du grand rêve de nous rapprocher de l’immortalité.» En attendant, les cellules et les tissus qu’on élabore au LBB ont déjà une grande utilité pour l’étude en laboratoire de plusieurs maladies.
Environ 80% des travaux du Laboratoire portent sur les tissus vasculaires. «Nous avons 900 km de vaisseaux dans le corps, rappelle le directeur; il est logique de penser que des pépins vont se produire quelque part là-dedans au moins une fois dans notre vie.»
La technique du LOEX
Au Laboratoire d’organogénèse expérimentale (LOEX) aussi, on travaille pour le futur. Mais avec une méthode différente, qui ne fait appel à aucun matériau externe comme le collagène.
Grâce à une technique d’autoassemblage mise au point par le Laboratoire, ce sont les cellules elles-mêmes qui construisent leur échafaudage à partir d’un ensemencement de fibroblastes (cellules du tissu conjonctif) et d’acide ascorbique (vitamine C). Cette technique a déjà donné lieu à plusieurs grandes réalisations dont l’une, aujourd’hui d’application courante, a d’abord été pratiquée seulement à partir des cellules épithéliales humaines (sans fibroblastes) que cultivait déjà le Laboratoire d’organogénèse à ses débuts.
En effet, c’est en 1986 qu’a été réalisée, sur un grand brûlé, la première greffe canadienne d’épiderme entièrement produit in vitro à partir des propres cellules du patient. Depuis, les équipes du Laboratoire se déplacent dans différents hôpitaux de Montréal, d’Ontario et de l’est du Canada pour pratiquer ces transplantations (une quinzaine par année).
La technique a beaucoup évolué, selon le directeur et fondateur du LOEX François Auger4, au point où l’on réussit maintenant à produire une peau bilamellaire, c’est-à-dire non seulement l’épiderme, mais aussi la couche sous-jacente qu’est le derme.
Cela constitue une première mondiale, souligne Lucie Germain5, coordonnatrice scientifique de l’organisme. La peau bilamellaire n’est pas encore homologuée par Santé Canada, mais déjà une quinzaine de patients ont pu en profiter grâce à un programme d’«accès spécial».
La prochaine grande étape sera de produire une peau complète, incluant l’hypoderme (la couche profonde) et, ultimement, des glandes, des poils, des vaisseaux sanguins et une innervation. Des vaisseaux sanguins microscopiques (les capillaires) et une peau vascularisée ont d’ailleurs déjà été créés séparément –deux premières mondiales en 1998–, mais n’ont pas encore été transplantés chez des humains. En attendant de s’en servir à des fins cliniques, on les utilise beaucoup, au lieu d’animaux de laboratoire, en recherche fondamentale sur différentes maladies, dont le cancer.
Des neurones dans le cerveau
Tous les travaux du Laboratoire d’organogénèse ont d’ailleurs ce double objectif d’application clinique et de recherche fondamentale avec les modèles réalisés intra-muros. À part les greffes de peau, les transplantations restent encore à venir, mais les équipes du LOEX avancent sur plusieurs fronts. En 2007, l’une de ces équipes a réussi à «construire» des neurones.
«Nous n’avons pas encore d’entités neuronales complètes avec des millions de neurones ensemble, ce qui pourrait prendre beaucoup de temps, explique François Auger. Mais dans quelques années, il sera envisageable d’implanter des neurones séparés dans le cerveau, sous forme de thérapie cellulaire.» Ou de réparer des nerfs, ajoute Lucie Germain.
Bronches, vessie, ligaments et valve cardiaque sont autant d’autres constructions à base de cellules souches sur lesquelles travaille le LOEX. Ainsi que la cornée, en fait l’épithélium de la cornée –la couche superficielle de l’oeil–, dont la transplantation chez des patients pourrait devenir courante d’ici un an. De quoi redonner la vue à des personnes presque aveugles. Les résultats des premières transplantations, effectuées depuis 2012, ont été dévoilés à la presse le 14 avril 2014.
Pour la cornée, les cellules souches sont prélevées dans le blanc de l’œil sain, tandis que des échantillons de peau fournissent les cellules souches de l’épiderme et de plusieurs autres organes, dont les neurones. Mais le tissu adipeux, le gras, est aussi largement pourvoyeur de cellules souches, qu’on utilise notamment pour la construction de l’hypoderme. L’espoir, avec les cellules du gras, réside surtout du côté de la reconstruction d’un sein vivant après une mastectomie, une opération qui ferait aussi appel à l’expérience acquise en vascularisation. Mais pas avant une vingtaine d’années, précise François Auger.
4 François Auger est aussi directeur scientifique du centre de recherche FRSQ du Centre hospitalier affilié universitaire de Québec (CHA). ↩
5 Elle est également directrice de l’axe médecine régénératrice du Centre de recherche du CHU de Québec. ↩
Longévité et qualité de vie Dans un horizon plus court, de 5 à 15 ans, il est pensable qu’on remplacera certains organes relativement simples grâce au génie tissulaire, estime le directeur du LOEX. « Et pour des organes entiers aussi complexes que le foie, les reins ou le cœur, il faudra peut-être de 20 à 50 ans. Mais on va y arriver!» François Auger entrevoit même la possibilité de faire repousser un doigt coupé, un jour. Et la beauté, avec la médecine régénératrice, considère-t-il, c’est que le tissu greffé suit le développement de la personne: le doigt repoussé ou une vessie implantée sur un enfant vont grandir en même temps que lui.
Dans un horizon plus court, de 5 à 15 ans, il est pensable qu’on remplacera certains organes relativement simples grâce au génie tissulaire, estime le directeur du LOEX. « Et pour des organes entiers aussi complexes que le foie, les reins ou le cœur, il faudra peut-être de 20 à 50 ans. Mais on va y arriver!» François Auger entrevoit même la possibilité de faire repousser un doigt coupé, un jour. Et la beauté, avec la médecine régénératrice, considère-t-il, c’est que le tissu greffé suit le développement de la personne: le doigt repoussé ou une vessie implantée sur un enfant vont grandir en même temps que lui.
Bien sûr, génie tissulaire et médecine régénératrice n’apporteront pas l’immortalité aux humains. Peut-être un allongement de la longévité, toutefois? Sans doute pas au-delà de 120 ans, pense Diego Mantovani.
Pour Lucie Germain, l’important s’avère moins la longévité que la qualité de la vie: «Mon but premier avec la médecine régénératrice n’est pas de prolonger la vie, mais d’améliorer les conditions de vie d’un aveugle, d’un paraplégique ou d’un grand brûlé.»
N’empêche. «Ce qu’on réussit à faire aujourd’hui était impensable voilà 20 ans, témoigne M. Mantovani. Qui sait où nous en serons dans 20 ans encore?»
Publié le 9 avril 2014










Publié le 6 mai 2014 | Par Nicole Roy
Bravo!
Note : Les commentaires doivent être apportés dans le respect d'autrui et rester en lien avec le sujet traité. Les administrateurs du site de Contact agissent comme modérateurs et la publication des commentaires reste à leur discrétion.
commentez ce billet